中國疫苗行業研究系列I
疫苗的過去、現時及未來
世界上最古老的生物技術藥物
疫苗或是世界上古老的生物藥物。1796年,一位英國醫生利用牛痘膿包中的物質成功為患者接種天花疫苗(天花由天花病毒引起)。至1900年,人類已經研製出天花疫苗及狂犬病疫苗兩種病毒疫苗、以及鼠疫疫苗、傷寒疫苗及霍亂疫苗三種細菌疫苗。
免疫接種(或疫苗接種)或許是最具成本效益的公共衛生干預措施,據說每年可預防200萬至300萬例死亡。
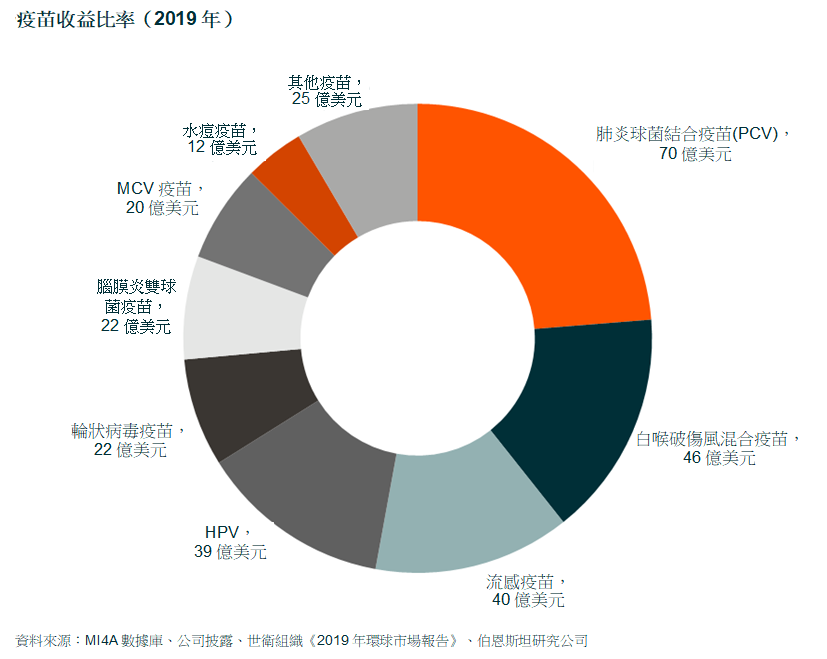
2020年,疫苗市場規模達約350億美元(2000年約為50億美元),並以約9%複合年增長率的增速持續增長。過去二十年間,市場規模增長的主要推動因素其一為關鍵疫苗的推出,包括5價疫苗DTP-HepB-Hib(2004年)、腦膜炎雙球菌疫苗(2005年)、兒童肺炎球菌疫苗(HPV)(2000年)、人類乳頭瘤病毒疫苗(2006年)及輪狀病毒疫苗(2006年),其二為疫苗的普及率增加。
疫苗及其漫長生產流程
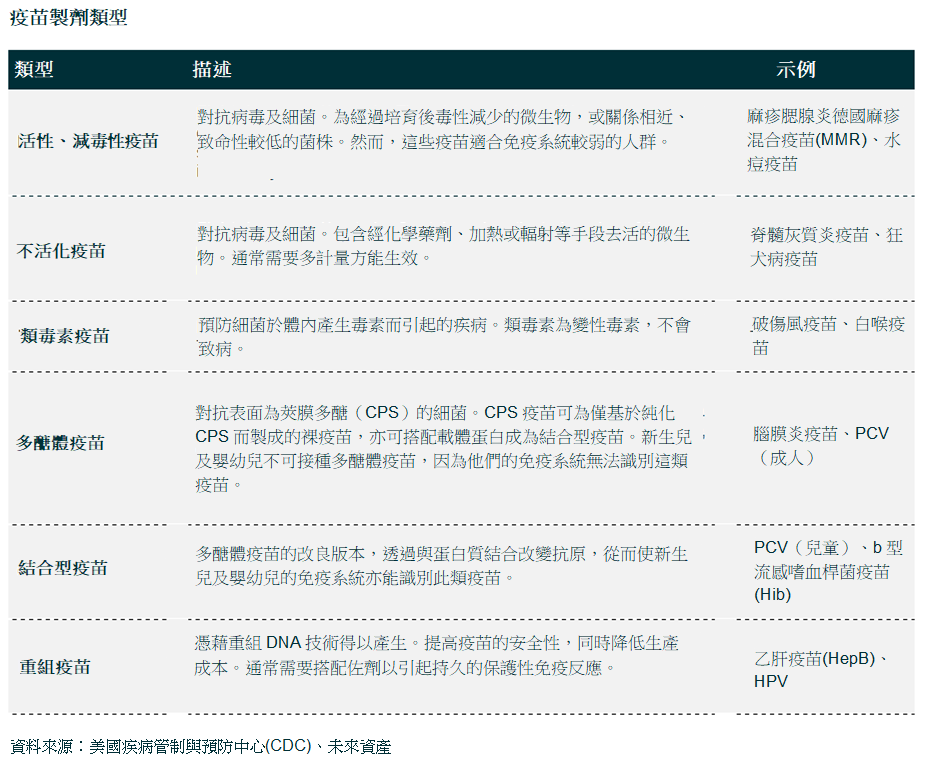
疫苗是一種生物製劑,使受體能對一種特定疾病產生免疫力。疫苗是由基於致病微生物(弱化/失能形式的病原體,或毒素/表面蛋白純化形式的病原體)的製劑製成。疫苗刺激人體的主要免疫反應,從而產生抗體。
疫苗是複雜的生物產品,可以說是經過一套複雜流程才能得出的產物。其中包括抗原,一種大而複雜的分子,於天然可變的生物過程中產生,因此很難表徵抗原。這一可變性意味著生產質素穩定的疫苗需要精湛的製作工藝及測試技術。對專業技術及有關成本的需求為潛在的新參與者設立了較高的行業門檻,即使在非專利疫苗領域亦是如此。
疫苗的生產需要很長的前置時間(8至36個月),生產過程中的每一個步驟及變量都要標準化,且必須受到管控、驗證及測試。不同的疫苗成分可能於多個不同的產地生產,並需要進行數百次質素控制測試。對高度無菌及溫控環境(標準冷藏鏈為2-8°C)的要求進一步提高了生產的複雜性。以美國為例,美國食品藥品監督管理局規定,新疫苗工廠須至少營運兩年後方可向市場投放產品,以證明工廠具備無菌、無外來微粒物質的環境、以及具備疫苗重組及提升疫苗穩定性所需的凍乾工藝。這不僅提高了行業准入門檻(由於要求大量啟動資金及較高專業技術),還提高了疫苗價格。
寡頭型市場
儘管疫苗市場十分具吸引力,但全球疫苗市場的新加入者十分有限。我們認為原因如下:
- 疫苗開發的前置時間很長。
- 製作流程複雜。美國食品藥品監督管理局(FDA)、歐洲藥品管理局(EMA)、世界衛生組織、各國家監管機構通常每年對疫苗設施進行20至25次實地檢查,同時質量保證團隊亦進行內部審查。
- 複雜且(與常規藥物)不同的分銷渠道
- 複雜的法規。以美國為例,美國食品藥品監督管理局規定,新疫苗工廠須至少營運兩年後方可向市場投放產品,以證明工廠具備無菌、無外來微粒物質的環境、以及具備疫苗重組及提升疫苗穩定性所需的凍乾工藝。
按價值計算,前四大公司貢獻了全球疫苗市場逾80%的份額。且60%的收入來自於四大疾病。而就銷量而言,跨國公司約佔總銷量的30%,因為領先的公司更注重銷售較新一代的、創新型藥物,而規模較小的國內公司關注老一代、創新程度較低的疫苗產品,並且僅專心耕耘本土市場。
mRNA技術的廣闊前景
mRNA是一種單鏈分子,它將遺傳密碼從細胞核中的DNA傳遞至核醣體(細胞內合成蛋白質的場所)。mRNA藥物簡單來說是向體內細胞發出的一組指令,刺激特定蛋白質的合成從而幫助預防或對抗疾病。很多公司已研發出或正努力研發技術及方法,從而生產能被細胞識別為體內合成的mRNA序列。
數家跨國公司與開發疫苗領域mRNA技術的公司訂立了合作關係。例如,輝瑞與BioNTech合作研發流感候選疫苗、默克在呼吸道合胞病毒領域與Moderna展開合作、同時賽諾菲亦與Translate Bio建立起合作關係。CureVac,與寶靈家殷格翰及禮來共同開發腫瘤產品,並與Genmab合作研發抗體。
Global X中國生物科技ETF,為您帶來機遇,可投資數十家深植於中國生物技術領域之公司的機遇,以及把握中國疫苗行業發展的機遇。